![]() источник: tiktokk.ru
источник: tiktokk.ru
МОСКВА, 27 сен — РИА Новости, Альфия Еникеева. Недавно обнаружена еще одна предполагаемая мутация, которая ведет к раннему старению, — в гене nsd1. Известно уже несколько десятков таких генов. Гипотетически блокировка этих участков генома могла бы замедлить старение и продлить жизнь. Но вмешательство в геном способно привести и к другим — неприятным последствиям. Впрочем, ученых это не останавливает. Опыты по отключению генов старения проводятся сейчас сразу в нескольких лабораториях. Что из этого получается, рассказывает РИА Новости.
Молодые старики
Первая публикация о предполагаемом гене старения появилась в 1996 году в журнал Science. Ее авторы, ученые из Японии и США, изучали людей с синдромом Вернера — при этом заболевании организм изнашивается в два раза быстрее, чем обычно, и человек в сорок лет выглядит на восемьдесят. Исследователи обратили внимание на мутацию в гене WRN, расположенном на восьмой хромосоме. Предположили, что из-за нее нарушаются какие-то важные процессы в организме, и это ускоряет старение.
Через несколько лет догадка отчасти подтвердилась. Синдромом Вернера действительно страдают только те, у кого есть две копии мутантного гена WRN. Однако его вряд ли можно считать геном старения в прямом смысле: это посредник, влияющий на другие участки ДНК.
Дело в том, что WRN производит белок, поддерживающий структуру и целостность человеческой ДНК. Любые его дефекты (а они неизбежны, если в этом гене есть мутация) изменяют механизмы репликации и восстановления поврежденной молекулы. Это, в свою очередь, сказывается на работе других участков генома, в том числе связанных со старением.
Старше своих лет
Под подозрение попал ген меланокортинового рецептора первого типа (MC1R), открытый недавно нидерландскими, британскими и китайскими учеными. Они соотнесли геномы 2693 пожилых людей с внешними проявлениями возраста, отраженными на их фотографиях.
Проанализировав более восьми миллионов однонуклеотидных полиморфизмов — отличий в последовательности ДНК размером всего в один нуклеотид, установили: те, что находятся в гене MC1R, связаны с внешними признаками старения. Так, люди с двумя копиями мутантного варианта MC1R выглядят в среднем на два года старше фактического возраста.
Два года — вроде бы немного. Однако если носители мутации курят, слишком часто посещают солярий и ведут не самый здоровый образ жизни, то разрыв между видимым и реальным возрастом увеличивается, предупреждают авторы исследования.
Похожим образом действует и мутантный вариант гена nsd1. По данным канадских и британских ученых, те, кто получил по его копии от каждого из родителей, стареют быстрее ровесников.1
Заразное старение
В процессах старения заметную играет роль также ген CD36, обнаруженный в прошлом году американскими генетиками. Судя по всему, он отвечает за прекращение деления клетки, что сигнализирует о ее скорой гибели.
Исследуя стареющие клетки, ученые обратили внимание на необычную активность CD36. Чтобы изучить ее детальнее, провели два эксперимента. В первом модифицировали 15 процентов молодых здоровых клеток в культуре так, что ген CD36 работал эффективнее. В результате те перестали делиться и проявляли явные признаки старения. Более того, заразили этим остальные клетки в культуре с нормальным геном.
Во втором опыте генетики некоторое время продержали в питательном растворе культуру стареющих клеток, затем вместо нее поместили более молодые клетки. Те, в свою очередь, внезапно прекратили делиться, словно переняв качества прежних «жильцов». Это подтверждают эксперименты на фибробластах кожи и легких. Но почему так происходит, непонятно, признают авторы исследования.
![]()
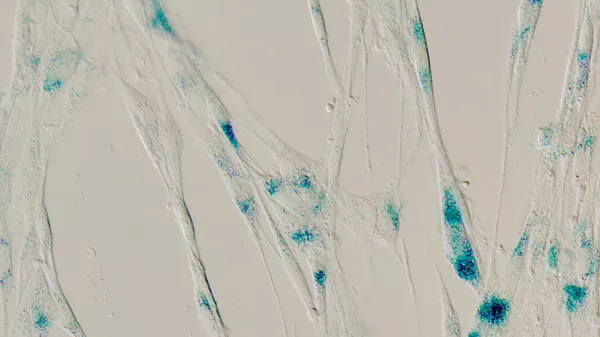
© Darleny Lizardo/Alan Siegel/University at Buffalo North Campus Confocal Imaging Facility
Стареющие клетки под микроскопом: синим цветом обозначены области повышенной экспрессии гена CD36
Ген отключил, молодость продлил
Швейцарские ученые экспериментируют с геном PUM2. В молодых клетках производимый им белок необходим для синтеза пептидов. А вот в более пожилых он превращается в серьезную помеху: его молекулы сбиваются в клубки и мешают РНК передавать инструкции из ядра в те части клетки, где собираются белки.
Так, одна из «жертв» PUM2 — вещество MFF, важное для утилизации поврежденных митохондрий. Дело в том, что содержимое этих клеточных энергостанций, за исключением АТФ и продуктов жизнедеятельности, никогда не покидает их пределов. Когда же митохондрии изнашиваются, в них образуются своеобразные дыры, через которые в цитоплазму клетки просачиваются агрессивные молекулы, повреждающие ДНК клетки и вызывающие перебои в ее работе. Молодые клетки справляются с такими авариями в том числе благодаря MFF, расщепляя митохондрии на части и переваривая поврежденные фрагменты. В пожилых клетках этому препятствует PUM2. В результате клетки стареют быстрее и погибают.
Если же PUM2 вовремя отключить или вырезать из ДНК, старение замедлится, предположили ученые и заблокировали этот ген у червей-нематод. Митохондрии во всех клетках помолодели, а животные прожили значительно дольше, чем их немодифицированные собратья. А вот с мышами этот прием оказался не столь эффективен. Митохондрии помолодели только в клетках кишечника.
На очереди — опыты с культурами человеческих клеток. Исследователи надеются найти более безопасный способ сократить количество белка, производимого PUM2, не редактируя геном.
![]() нобелевку за изучение аутофании в клетке. Так вот следствием ( на прямую Ёси такой выаод не делает ) лечебное голодание способствует аутофоагии разрушенных клеточных структур ( мусора) в том числе осколков миотохондрий. Кроме того стимуляция клеточной аутоагии позволяет клетке оптимизировать работу — избавлясь от лишних не эффективных структур.
нобелевку за изучение аутофании в клетке. Так вот следствием ( на прямую Ёси такой выаод не делает ) лечебное голодание способствует аутофоагии разрушенных клеточных структур ( мусора) в том числе осколков миотохондрий. Кроме того стимуляция клеточной аутоагии позволяет клетке оптимизировать работу — избавлясь от лишних не эффективных структур.