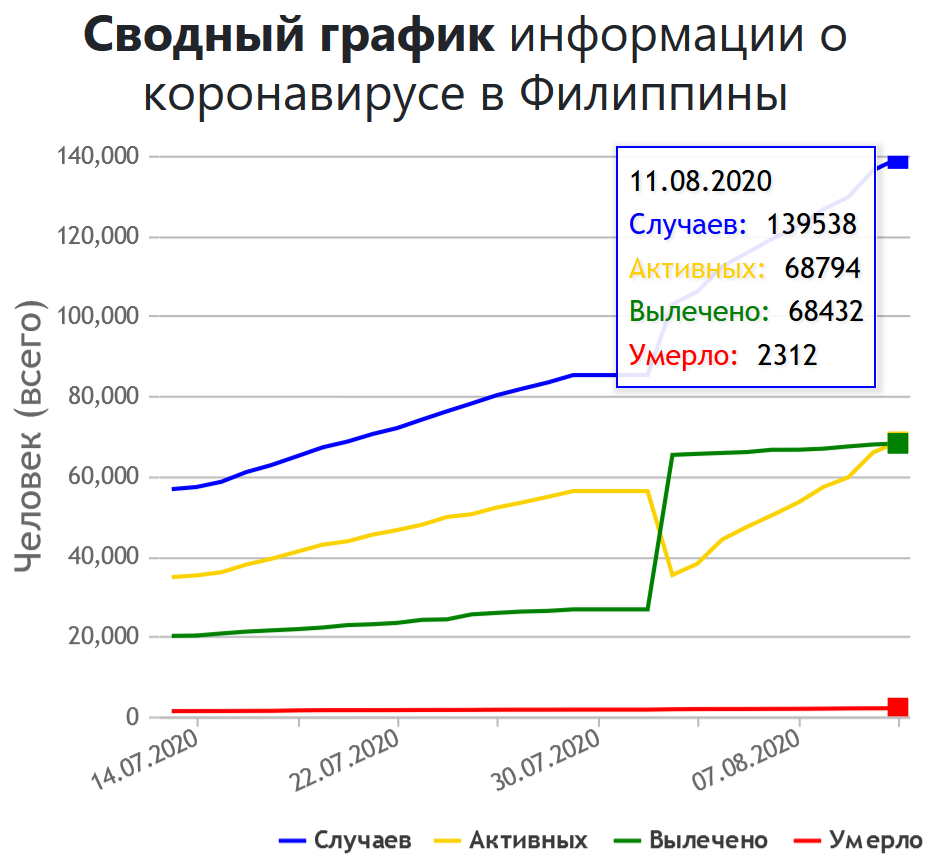
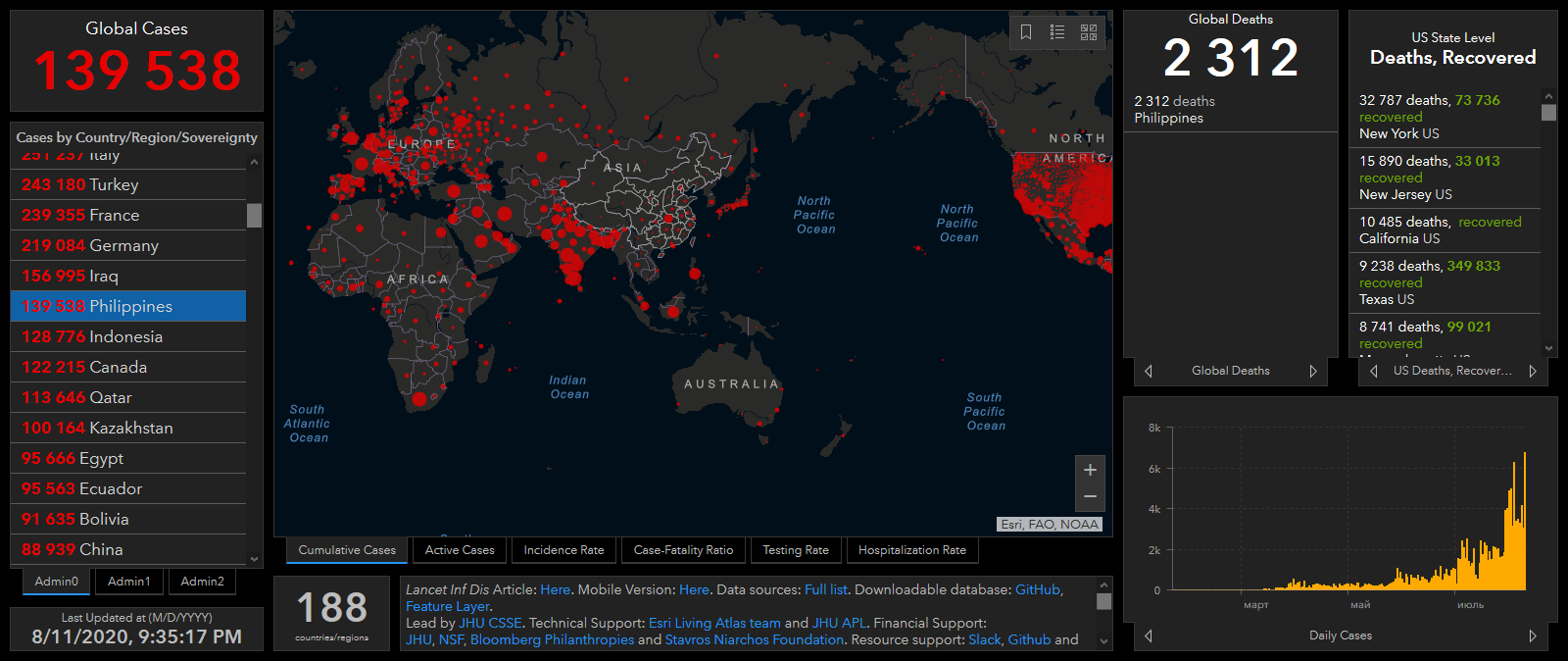
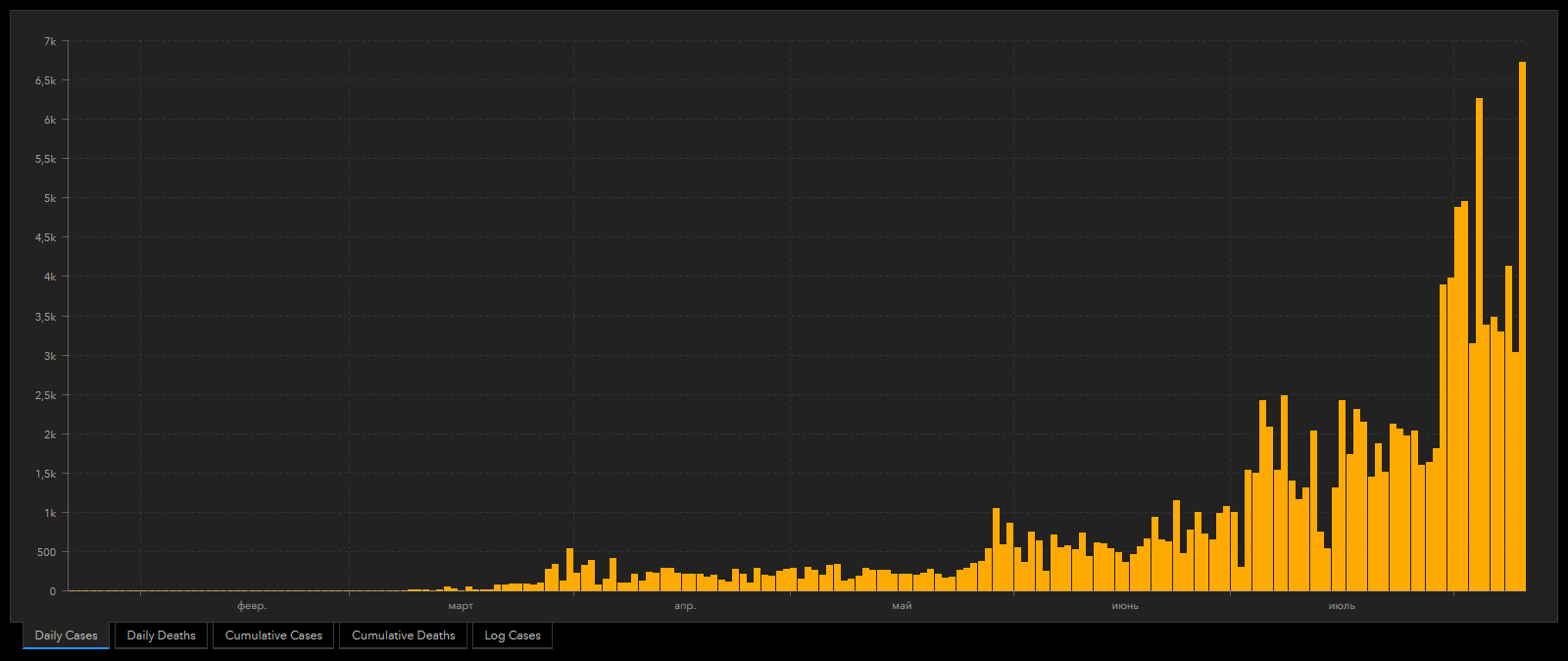
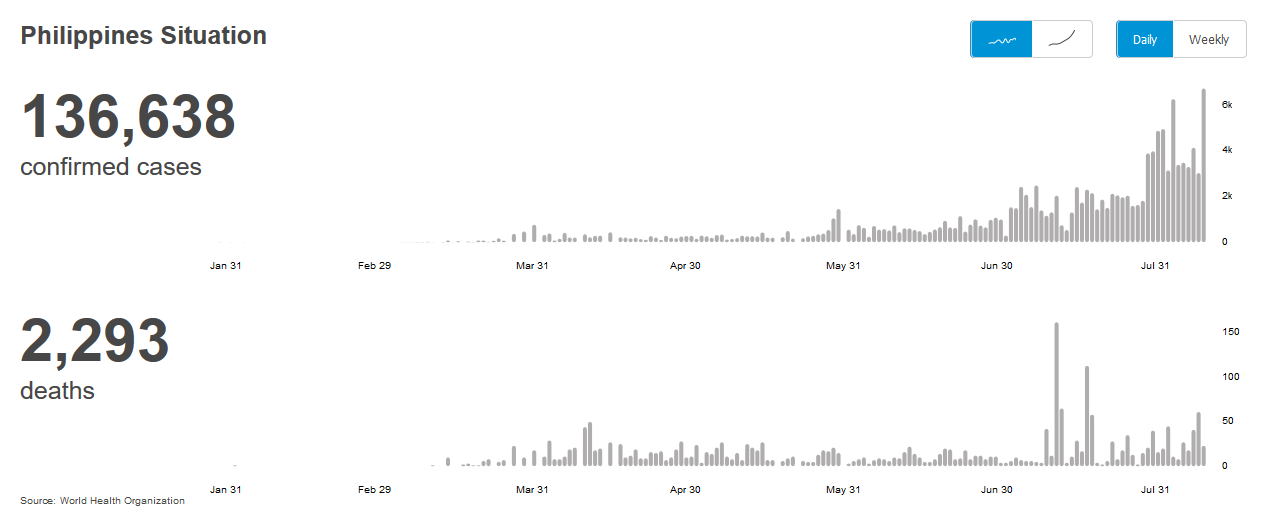
Президент Филиппин Родриго Дутерте вызвался первым на себе испытать российскую вакцину против коронавируса.
не звучит. Лучше так.
Президент Филипин с говорящей фамилией Дурерте вызвался первым испытать на себе вакцину, не прошедшую полный цикл испытаний...
Она прошла полный цикл испытаний, регистрацию, более того, ею уже вакцинируют.
Кроме того, Центр Чумакова подал заявку на поставку вакцины от коронавируса
«Мы подали заявку на участие в международном тендере ВОЗ по поставкам вакцины. Стоит отметить, что Центр имени Чумакова ― единственный в России поставщик вакцин, прошедший аудит ВОЗ и экспортирующий вакцины более чем в 50 стран по всему миру», ― рассказал он агентству.
При этом Ишмухаметов подчеркнул, что поставки на международный рынок инактивированной цельновирионной вакцины для профилактики COVID-19 будут возможны только после того, как будут удовлетворены потребности в этой вакцине в России.
кто такой Чумаков был, кто его дети, где работают, какова процедура в ВОЗ и пр. — материал для твоего ликбеза, но тебе надо начинать с чего попроще: с детского сада.
Не проходила полный цикл, не надо врать.
Минздрав РФ зарегистрировал первую российскую вакцину от нового коронавируса, созданную в Центре имени Гамалеи. Регистрация пока «условная», завершены только две фазы испытаний из трех, однако полученных данных, по мнению Минздрава, достаточно, чтобы начать вакцинацию людей из групп риска.
Третья фаза испытаний российской должна начаться в ближайшие дни, но пока еще впереди. Однако в странах, где созданы остальные вакцины, регистрировать даже для ограниченного применения их пока не стали, за исключением КНР, где военным на год разрешили применять аденовирусную вакцину — видимо, для вакцинации военнослужащих. Россия действительно стала первой страной, которая одобрила вакцину и готова вакцинировать представителей групп риска до завершения третьей фазы испытаний (невзирая на опасения Ассоциации организаторов клинических исследований).
Я бы смог объяснить всю дурь и несуразность этих измышлений и вывертов даже малолетнему ребёнку, даже, наверное, придурок с N+1, несмотря на свое прозападное безумное подобострастие и сектантстство, раскраснелся бы и больше не писал такой абракадабры. Но, очень сильно сомневаюсь, что смогу объяснить тебе. Очень уж твоя история запущена.
И так, вот инструкция. Где в ней хоть намёк на то, что для госрегисирации не выполнен полный цикл исследований?
Факт регистрации является подтверждением полного цикла исследований.
Но, нет и не может существовать полного цикла исследований в отрыве от задач исследования. Это — то понятно или нет?...
Иными словами: выполнен полный цикл исследований ДЛЯ ЦЕЛЕЙ государственной регистрации вакцины на условиях инструкции по ее применению. Опять переспрошу: понятно ли это?
Теперь то, что должно быть понятно без особых пояснений. Ну, и чтобы глупость и ограниченность автора опуса была ясна. ЛЮБАЯ ИНСТРУКЦИЯ по применению препаратов СОДЕРЖИТ УСЛОВИЯ. ЛЮ- БА-Я. ЛЮБОГО МЕДИЦИНСКОГО ПРЕПАРАТА. Это обстоятельств позволяет утверждать, что любая регистрация «условна»? Очевидно, что нет. Это — абсурд.
Действительно, третья фаза не пройдена, но она нужна будет завтра. Одна, две, три или десять фаз исследований нужны — решать регулятору.
Почему в конкретном случае регулятор удовольствовался двумя фазами. Если не брать в расчёт требования всем понятные, то это — не совсем новая двухвекторная вакцина. Она создана на основе вакцины против Эбола (кстати, самой эффективной в Мире). Над этой вакциной работали три года, там уже все фазы давно пройдены.
Никакой «гонки» в этом нет. Это уже журналисты придумывают поводы для пиара и контрпиара. Англичане вообще капитально рискуют. Они производство вакцины стали разворачивать ещё до прохождения второй фазы. И говорят :«Да, мы рискуем, может она окажется неудачной, но мы верим, и вакцина нужна уже вчера».
Единственной целью является противоинфекционная безопасность в максимально сжатые сроки.
Сейчас «Вектор» делает «клинику, на подходе ещё несколько мощных вакцин, весной можно ожидать инновационную РНК -вакцину. Но, „уже вчера“ Вакцина необходима. Есть риск? Нет, абсолютно, но даже с учетом этого, вакцинация будет поэтапной и аккуратно, т. к. всего предусмотреть нельзя.
Фейспалмище.
Читай
Как говорится в материалах, опубликованных на сайте ГРЛС, вакцина «Гам-КОВИД-Вак» зарегистрирована по процедуре регистрации препаратов, предназначенных для примененияв условиях чрезвычайной ситуации и на основе ограниченных клинических данных. Поэтому ее применение разрешено «только в медицинских организациях, имеющих право осуществлять вакцинопрофилактику населения».
Гам-КОВИД-Вак — векторная двухкомпонентная вакцина на основе аденовируса человека. Вакцина прошла все необходимые испытания безопасности и эффективности на нескольких видах животных (грызуны и приматы), позже вакцина была испытана на двух группах добровольцев (по 38 человек в каждой).
Т.е. только 2 этапа вместо трех. И это написано на оф. сайте.
И да регистрация неполная. Полная будет только после третьего этапа.
grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=d494c688-0bc6-4c30-9e81-23f043ceb43e&t=
вот ссылка на удостоверение препарата
Ну, как я и предполагал: ты абсолютно утратил способность к мышлению.
Тебе уже все разжевали: это — гос. регистрация. Для какого применения, на каких условиях- неважно. Гос. регистрация означает полный цикл исследований. Пусть для ограниченного оборота, неважно. Именно для применения на условиях инструкции он полный.
Для гражданского оборота будет сделана третья фаза. Это тоже будет означать полный цикл исследований, но уже для гражданского оборота.
Ещё раз, для тех, кто на бронепоезде без запасных частей: цикл исследований определяется целями и задачами исследования. Если задача проверка клиники для целей госрегистрации с ограниченным оборотом (множество таких препаратов), то факт госрегистрации означает именно это: полный цикл исследований препарата с ограниченным оборотом в условиях ЧС в соответствии с ![]() постановлением Правительства РФ N441 от 3 апреля 2020 года Об особенностях обращения лекарственных препаратов для медицинского применения, которые предназначены для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайной ситуации и для организации оказания медицинской помощи лицам, пострадавшим в результате чрезвычайных ситуаций, предупреждения чрезвычайных ситуаций, профилактики и лечения заболеваний, представляющих опасность для окружающих, заболеваний и поражений, полученных в результате воздействия неблагоприятных химических, биологических, радиационных факторов
постановлением Правительства РФ N441 от 3 апреля 2020 года Об особенностях обращения лекарственных препаратов для медицинского применения, которые предназначены для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайной ситуации и для организации оказания медицинской помощи лицам, пострадавшим в результате чрезвычайных ситуаций, предупреждения чрезвычайных ситуаций, профилактики и лечения заболеваний, представляющих опасность для окружающих, заболеваний и поражений, полученных в результате воздействия неблагоприятных химических, биологических, радиационных факторов
Ну, шевельни же извилиной, черт бы тебя подрал! Мы не на обывательском просторечии употребляем «полный цикл исследований», когда речь о дефиниции применительно к НПА.
ты туповат. Не в силах прочитать официальные документы.
Соболезную, но мировая практика это три фазы клинических исследований. Было проведено всего две. Т.е. неполное исследование.
Учись читать, тебе это пригодится в жизни.
Ты зря с огнём играешь, уклоняясь от лечения. Прогрессирует. Невооруженным глазом видно даже случайным людям.
Твои проблемы с чтением печальны. Но это не так страшно как выпуск препарата не проверенного на побочки. А именно в третьей фазе выявляются побочные эффекты.
И ещё. Нет и не может быть такого понятия, как «неполная государственная регистрация». Это противоречит самому понятию, по его определению, как в общем, исходя из смысла акта, юридического механизма, так и в случае конкретном в соответствии со ст. 13 ФЗ РФ N61- ФЗ.
Также как неполнота исследований — основание отказа в госрегистрации. Поэтому, безграмотно говорить о неполноте исследований для целей госрегистрации зарегистрированного в установленном законом порядке, препарата. Это равносильно утверждению незаконности его госрегистрации. Но, он зарегистрирован в соответствии с законом и правилами, постановлением Правительства РФ, поэтому это — абсурдное и безграмотное заявление.